2026年4月28日,博彩公司排名评级网丁俊军团队联合西北大学孙士生团队、中山大学药学院毛洋团队在Nature Cell Biology上发表研究论文Nuclear N‑glycosylation maintains H3K9me3 heterochromatin and genomic stability,该研究首次报道多糖链位于细胞核内,并且维持H3K9me3异染色质和基因组稳定性,改写了“多糖链不存在细胞核内”的传统认识,开辟了多糖表观遗传学方向。

细胞核内多糖链的鉴定
该研究利用自主研发的StrucGP方法【4】,在干细胞、分化细胞等多种细胞中鉴定到N-糖链(一种通过糖苷键与蛋白质天冬酰胺残基共价连接的多糖链)可修饰内核膜蛋白(即N-糖基化修饰)。并通过免疫荧光、免疫电镜以及自主开发的多糖染色质免疫共沉淀测序技术(GlycoChIP-seq)证实了N-糖基化修饰位于细胞核内(图1)。

图1 细胞核内N-糖基化修饰的鉴定与验证策略
该研究通过内核膜蛋白的N-糖基化修饰位点突变、N-糖基化转移酶抑制剂处理等多种实验手段,证实细胞核内N-糖基化修饰可介导 H3K9me3 甲基转移酶 SETDB1 锚定至内核膜,进而维持核周 H3K9me3 异染色质修饰稳态与基因组稳定性,该研究提供了首个N-糖基化修饰的细胞核内功能。

图2 细胞核N-糖基化修饰维持异染色质与基因组稳定性
该研究表明,N-糖链在内质网中依赖经典的N-糖基化合成机器对内核膜蛋白进行修饰,随后在GTP酶介导的膜系统动态调控下完成扩散与转运,并经由核孔复合体进入核内膜,从而实现其在细胞核内的定位,该研究为多糖链在细胞内的转运提供了新途径。
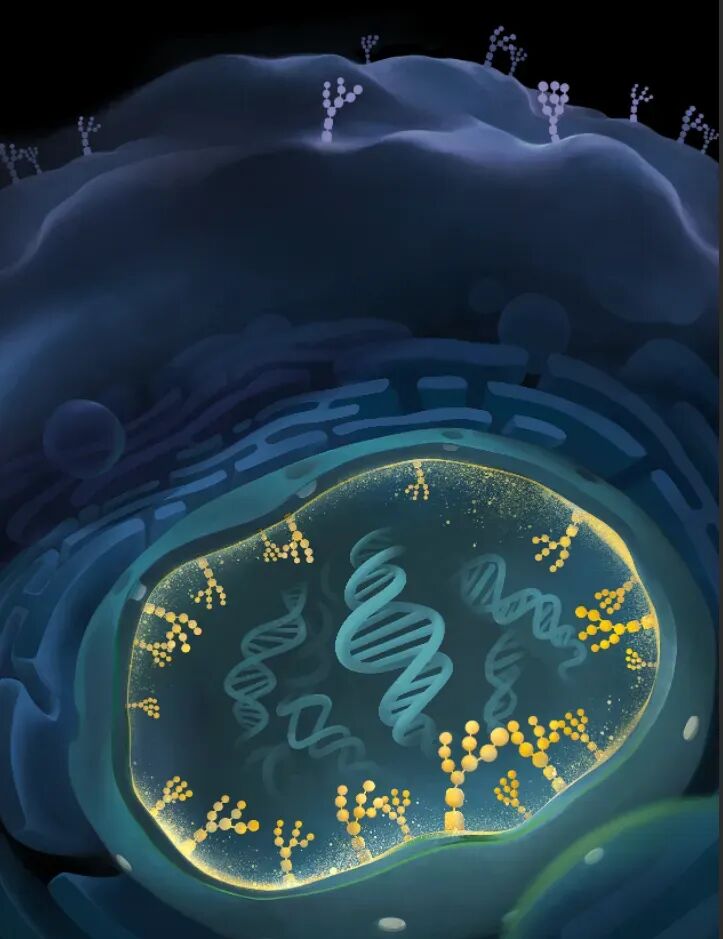
细胞核的N-糖基化修饰维持H3K9me3异染色质和基因组稳定性
1、首次证实了多糖链位于细胞核内,改写了经典认识;
2、揭示了核内多糖链维持染色质修饰稳态,特别是对异染色质形成的重要功能,开辟了多糖表观遗传学方向;
3、报道了多糖链维持基因组稳定性的首个核内功能,为多糖链的核内功能研究奠定了基础;
4、解析了多糖链定位在细胞核内的分子机制,为完善多糖链在细胞内转运提供了新认知。
至此,曾被认为止步于细胞核之外的多糖链,在经过内质网的加工与塑造后,跨越界限,悄然进入细胞核之中,参与到异染色质稳态的维持与基因组稳定性的守护之中。细胞核内潜藏的多糖调控网络仍待挖掘与解析,多糖链深耕核内的功能图景,远比过往认知更为广阔深邃,属于它的科研篇章,才刚刚启程。
中山大学唐秀晓、戴然然,四川大学卿莉及西北大学张知达为本文的共同第一作者。中山大学丁俊军教授、西北大学孙士生教授及中山大学毛洋教授为论文的通讯作者。感谢同济大学高绍荣院士、生物物理研究所朱冰院士等在论文完成过程中提供的指导和帮助。
原文链接://www.nature.com/articles/s41556-026-01941-9
1. Varki, A. et al. Essentials of glycobiology. Fourth edition. edn, (Cold Spring Harbor Laboratory Press, 2022).
2. Flynn, R. A. et al. Small RNAs are modified with N-glycans and displayed on the surface of living cells. Cell 184, 3109-+, doi:ARTN e2210.1016/j.cell.2021.04.023 (2021).
3. Schjoldager, K. T., Narimatsu, Y., Joshi, H. J. & Clausen, H. Global view of human protein glycosylation pathways and functions. Nat Rev Mol Cell Bio 21, 729-749, doi:10.1038/s41580-020-00294-x (2020).
4. Shen, J. C. et al. StrucGP: de novo structural sequencing of site-specific N-glycan on glycoproteins using a modularization strategy. Nat Methods 18, 921-+, doi:10.1038/s41592-021-01209-0 (2021).

